JAMA CONNECT--案例研究--医疗设备
借助 Jama Connect 加快安全有效的医疗器械和生命科学产品的开发速度
在医疗器械和生命科学行业,从以硬件为核心的设备向以软件为驱动的多样化产品转变,再加上硬件和生物武器,正在重塑设备及相关产品的开发工具和流程。用于医疗设备需求管理的 Jama Connect 是专为减少实现监管合规所需的工作量而设计的,它可以管理设备需求和相关风险的设计控制,简化监管提交和审计准备工作,并加快产品上市时间。
通过 Jama Connect,您可以
· 通过 Live Traceability™ 有效管理需求、风险、验证和确认
· 快速调整硬件、软件和生物are 产品开发团队的系统工程学科
· 简化监管呈件并符合行业标准

支持多重和混合产品开发流程 (PDP)
Jama Connect 提供了一个灵活的解决方案,可以管理您所有的产品开发方法。

Jama Connect 提供全面的解决方案,可简化整个设备、产品、系统和软件生命周期的产品开发流程。

Jama Connect 简化了设计历史档案/技术档案的审查周期和文档创建,是对质量管理系统的补充。
“Jama Connect 的自动化功能使我们能够高效地管理每次发布。该工具使我们能够减少生成可追溯性的人工流程,并将精力集中在对跟踪矩阵的审查上。效率和速度对于我们管理软件的节奏以及在市场上保持竞争力至关重要。
Sandhya Mitnala 质量与监管负责人
“有了审查中心,我们可以更循序渐进地进行审查,在审查过程的早期就能发现变更或需要修正的地方。因此,最终的成本会更低"。
Carmen Pazos 诊断部门研发、仪器高级经理
Jama Connect for Medical Device & Life Sciences Development 是一个功能强大的单一平台,供医疗器械团队管理针对器械要求和相关风险的设计控制,简化监管提交和审计准备工作,同时加快产品上市时间。它包含标准的医疗设备框架,支持关键的医疗设备软件标准和法规,包括
· 监管机构: FDA 21 CFR 820.30、21 CFR 11、EU MDR、EU IVDR
· 质量体系: ISO 13485
· 风险管理流程和方法 ISO 14971、IEC 60812
· 医疗软件开发: IEC 62304、AAMI TIR 45 和 SW 96
· 人为因素和可用性工程 He 75、IEC 62366
Jama Software 支持的医疗器械/生命科学领域包括医疗器械、诊断(IVD、LDT、RUO)、医疗器械软件、制药、生命科学等!
实时可追溯性
将高层次需求与更详细的子系统需求联系起来,确保在发布前进行适当的验证。
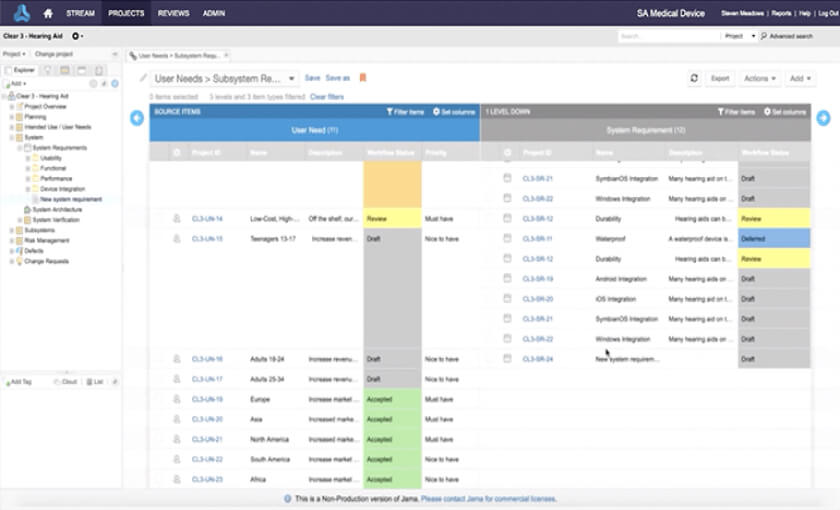
• 提高效率
• 推动一致性
• 降低组织风险
编写和维护需求,显示与相关上游和下游需求的联系
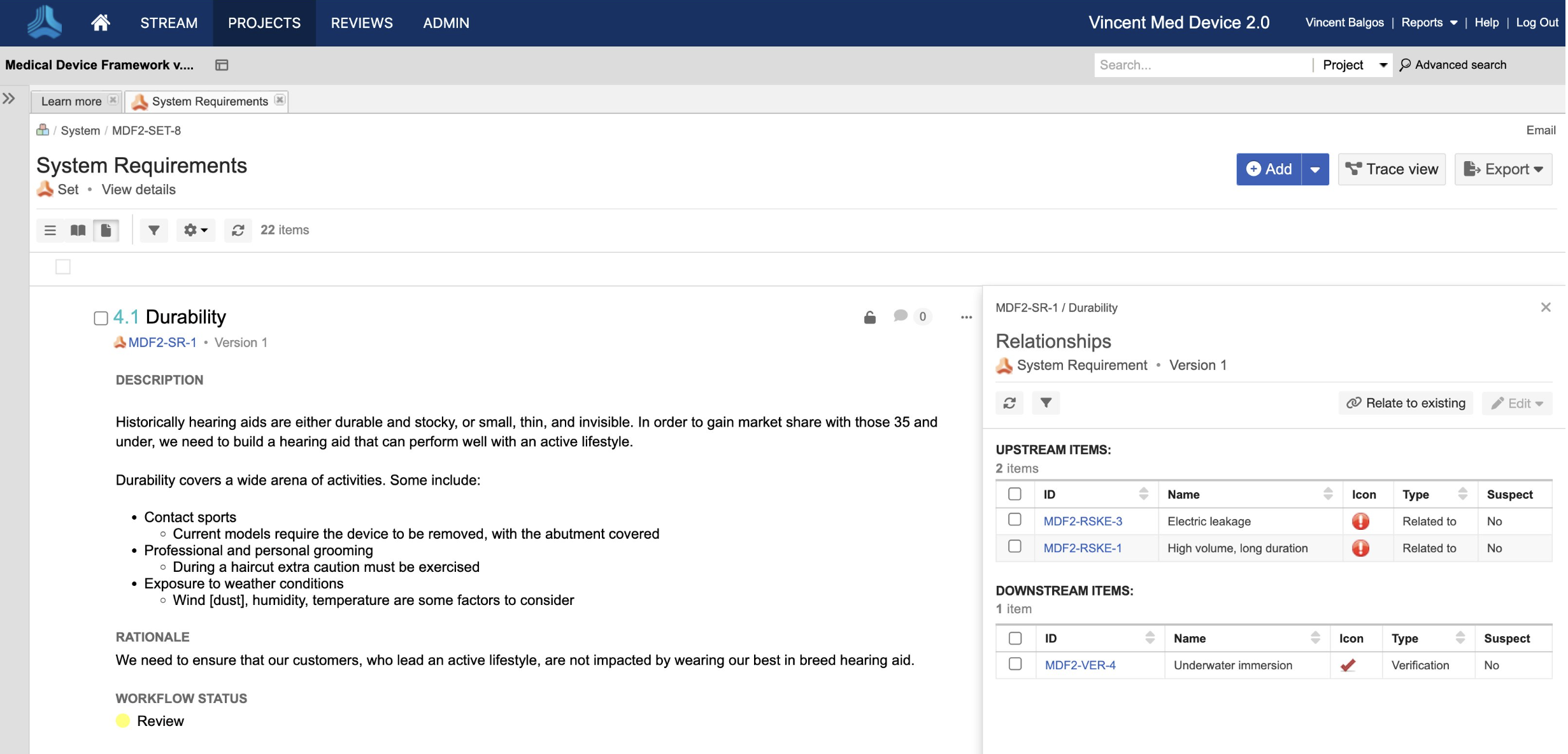
风险管理
建立医疗器械风险管理框架,确保质量并尽量减少设计变更。

• 符合 ISO 14971:2019 标准
• 在开发早期降低风险
• 支持合规之路
验证和确认
无缝管理用于验证和确认的测试用例的可追溯性。

• 提供符合法规和标准(如《联邦法规汇编》第 21 卷第 820.30 部分)的证据
• 管理用于验证和确认的测试用例的可追溯性
从资料库或其他项目中重复使用具有关系的常用项目,并同步查看不同时间的差异。

审查和批准
与企业的质量流程相结合,实现符合 FDA 21 CFR Part 11 的要求。

• 提高审查过程的参与度
• 在审查过程中尽早提供可见性
• 更快生成可用于电子签名的审批就绪内容
文档
设计跟踪矩阵是用于文档编制的预设格式报告示例
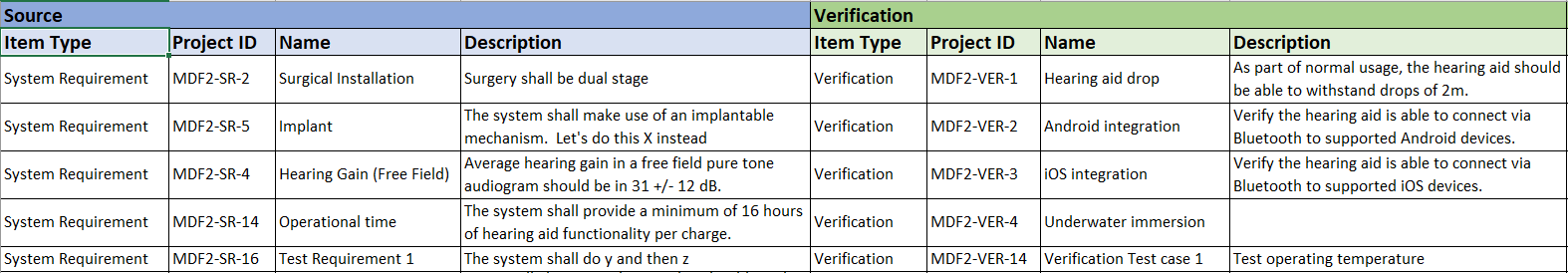
设计历史文件/技术文件
为您现有的质量管理体系制作高质量、可审核的 DHF/技术文档文件。

Jama Software 是该领域唯一能提供以下服务的供应商: SOC 2 类型 2 认证的应用程序和数据中心(其他供应商仅提供数据中心)、高于 99% 的 SLA(其他供应商为 95% 或更低)、无接触升级(其他供应商要求 IT 人员手动更新托管应用程序)、高可用性 SLA(其他供应商不提供)、灾难恢复 SLA(其他供应商不提供)。
通过 TÜV 南德意志集团的安全相关开发验证
根据 OWASP 最佳实践编写 Jama 软件代码
Jama Connect 服务器和应用程序均通过了 SOC2 类型 2 认证。
确保强有力的隐私管理实践
传输层安全(TLS)确保传输的数据安全加密